식품의약품안전처는 21일 외부 전문가가 포함된 최종점검위원회를 열고 녹십자가 지난 4월 12일에 수입품목 허가를 신청한 코로나19 백신 ‘모더나 코비드-19백신주’에 대해 임상시험 최종결과보고서 등을 제출하는 조건으로 수입품목허가를 결정했다.
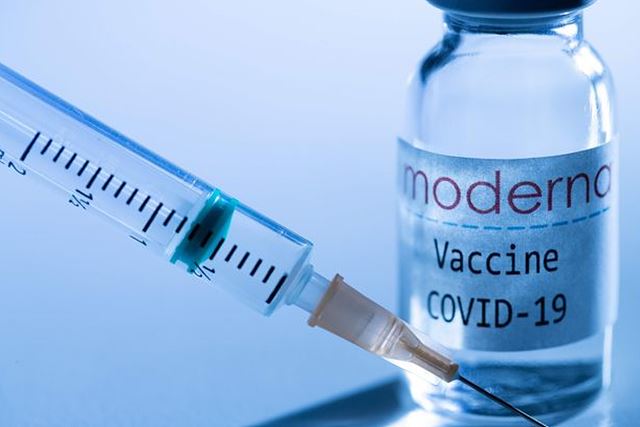
녹십자가 수입품목허가 신청한 ‘모더나 코비드-19백신주’는 미국 모더나가 개발한 mRNA 백신으로, 코로나19 바이러스 항원 유전자를 mRNA 형태로 주입하여 체내에서 항원 단백질을 합성하고, 이 단백질이 중화항체의 생성을 유도함으로써 코로나19 바이러스가 인체에 침입했을 때 바이러스를 중화해 제거하는 기전의 백신이다.
RNA(Ribonucleic acid)는 유전자 정보를 매개, 유전자 발현 조절 등의 역할을 하는 세포의 핵 속에 있는 두 종류의 핵산 중 하나다.
이 약의 효능‧효과는 18세 이상에서 코로나19의 예방이며 용법‧용량은 해동 후 0.5 mL을 1회 접종 후 4주 후에 추가 접종하고 보관조건은 냉동(영하 25~15℃)에서 7개월, 냉장(2~8℃) 1개월입니다.
‘모더나 코비드-19백신주’는 국내에서 네 번째, mRNA 백신으로는 국내에서 두번째로 허가받는 백신이며 유럽(EMA), 미국 등 39개 국가와 WHO에서 조건부 허가 또는 긴급사용승인을 받았다.
안전성 최종점검위원회는 보고된 이상사례가 대부분 백신 투여와 관련된 예측된 이상사례로 전반적으로 양호하다고 판단했다.
흔하게 나타난 이상사례는 주사부위 통증, 피로, 두통, 근육통, 관절통, 오한, 메스꺼움/구토, 림프절병증, 발열, 주사부위 부종, 홍조 등이었으며, 증상은 대부분 경증에서 중간 정도 수준으로 백신 접종 후 며칠 내에 소실됐다.
아울러 임상시험의 모든 등록대상자 3만 351명 중 백신군 1.0%(147명), 대조군 1.0%(153명)에서 ‘중대한 이상사례’가 보고되었고, 백신 투여와 관련성을 배제할 수 없는 ‘중대한 약물이상반응’은 얼굴 부종 등 9건이었으며, 임상시험 자료 제출시점에는 대부분 회복중이었다. 또한 얼굴 부종은 사용상의 주의사항에 반영하였다.
얼굴부종(facial swelling, 얼굴 부어오름)은 필러시술 경험이 있는 백신 투여자에서 발생하였으며, 임상시험 자료 제출시 2건 모두 회복중이었다.
최종점검위원회는 이러한 결과를 토대로 백신의 안전성이 전반적으로 양호하지만 2차 투여 후 더 많은 통증, 피로, 오한 등 접종 시에 예측되는 사례 발생이 증가하는 경향이 있음을 사용상의 주의사항에 반영하도록 했다.
BEST 뉴스
-
![[단독] 강남 'ㄸ 치과'… 갑질 논란 이어 이번엔 수면마취 사망까지](/data/news/202601/news_1769440952.1.jpeg)
[단독] 강남 'ㄸ 치과'… 갑질 논란 이어 이번엔 수면마취 사망까지
서울 강남역 인근의 한 대형 임플란트 전문 치과에서 수면마취 시술을 받던 70대 여성이 끝내 사망하는 사고가 일어났다. 해당치과 건물(사진출처=구글 갈무리) 최근 일부 치과의 무분별한 수면마취 실태를 연속 보도해 온 MBN 취재로 드러난 이번 사건... -

‘판타지오’82억 불복 속 … 남궁견의 수백억 베팅
차은우의 ‘200억 원대 세금 의혹’이 확산된 지 채 열흘도 안 돼 김선호까지 유사한 논란에 휩싸이면서, 두 배우가 몸담았던 판타지오는 ‘아티스트 리스크’와 ‘세무 리스크’가 한꺼번에 몰려든 형국이 됐다. 이미지 출처=판타지오 누리집 김선호 건은 “가족 법인을 ... -

재고를 신상품으로 둔갑… ‘K-명품’ 이라는 우영미, ”택갈이 보다 심하다“
우영미(WOOYOUNGMI)를 둘러싼 논란이 단순한 '디자인 변경' 수준을 넘어 소비자 기만 논쟁으로 번지고 있다. 핵심은 같은 해 상·하반기 상품으로 판매된 두 후드 티셔츠다. 우영미는 지난해 하반기 '블랙 플라워 패치 후드 티셔츠’(정가 52만 원)를 출시했는데, 이 제품이 같은 해 상반기 출시된 '블랙 ... -

60억 원 배임·횡령’ 박현종 전 bhc 회장, 공판 앞두고 ‘전관 초호화 변호인단’ 논란
60억 원대 배임·횡령 혐의로 기소된 박현종 전 bhc 회장이 다음 달 4일 첫 공판을 앞둔 가운데, 전직 특검보와 부장판사 출신 변호사들이 대거 포진한 이른바 ‘초호화 전관 변호인단’을 꾸린 사실이 알려지며 논란이 커지고 있다. 박현종 전 bhc 회장 사진출처=연합뉴스 ... -
![[단독] 승무원 스타벅스 “민폐 논란”의 진실은?](/data/news/202602/news_1770710766.1.jpg)
[단독] 승무원 스타벅스 “민폐 논란”의 진실은?
광화문 일대 스타벅스 매장을 둘러싼 ‘승무원 민폐 논란’이 거세다. 기사의 이해를 돕기위한 AI 생성 이미지입니다 대형 가방과 서류가 매장 곳곳에 놓인 사진과 영상이 확산되자, 기사 제목과 댓글에는 곧바로 '아시아나항공 승무원’, ‘직원 민폐’라는 표현이 따... -

‘선분양 제한’ 논의에 GS건설 긴장… 재무 부담 우려
GS건설 주거 브랜드 '자이' [GS건설 제공/연합뉴스] 정부가 건설사 영업정지 처분과 연동되는 선분양 제한 규제를 실제로 적용할 가능성이 커지면서, GS건설이 대형 건설사 가운데 첫 사례가 될 수 있다는 관측이 나온다. 구조물 붕괴와 현장 사망 사고 등 안전 논란이 반복...









![[단독] “주인 죽었다”는 부고장에 거짓말까지 …](/data/news/202602/news_1770709987.1.jpg)